CMA认定条件有哪些?2025最新标准
CMA认定条件包括法人资格、人员配备、设备场所、管理体系和公正性要求。基于2023版评审准则和2021年管理办法,本文详解2025最新标准要点、人员授权签字人要求及设备溯源,帮助检验检测机构高效自查和申请资质认定。

CMA认定条件包括法人资格、人员配备、设备场所、管理体系和公正性要求。基于2023版评审准则和2021年管理办法,本文详解2025最新标准要点、人员授权签字人要求及设备溯源,帮助检验检测机构高效自查和申请资质认定。

本文分享三个真实案例(基于行业经验匿名处理),涵盖新能源、环境检测和医学领域,剖析申请流程、挑战及经验,帮助更多实验室高效获得CNAS认可。

一份完整的设备校准证书应该包含哪些内容?本文基于CNAS-CL01:2018和ISO/IEC 17025:2017,详解证书12项必备元素,包括机构信息、校准结果、不确定度和溯源声明。提供编制规范、实操步骤和常见问题解决,帮助实验室确保合规,提升评审通过率。
本文详解CNAS实验室LIMS系统选型指南,基于GB/T 27025-2019、ISO/IEC 17025:2017及CNAS-RL01:2025,涵盖ISO兼容、防篡改电子记录、审计追踪、多场所管理等关键功能,及需求评估、调研POC、合同实施等流程,提供避免误区策略,助力实验室缩短3-6个月周期,成功率100%,实现数据追踪效率翻倍,抓住检测市场超5500亿元规模、年增长9%-13%的机遇。

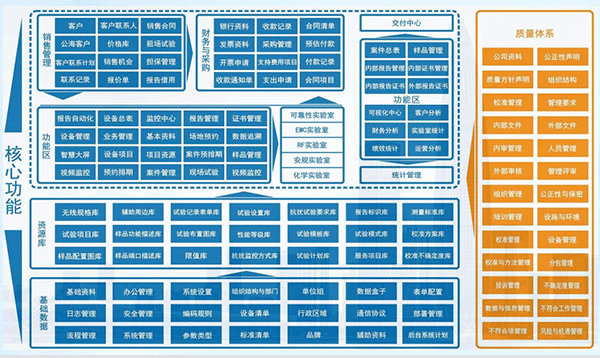
智慧实验室管理系统是检验检测行业数字化转型的创新解决方案。本文介绍系统如何应对市场竞争、合规压力和技术变革,通过自动化流程和AI智能体实现无纸化作业、实时监控和数据驱动决策。详解核心功能模块,包括销售项目管理、质量体系和实验运维,以及实施路径和未来收益,帮助实验室从传统模式转向智慧自驱动生态,提升效率与竞争力。

CNAS实验室LIMS系统选型指南详解。本文阐述CNAS认可实验室对LIMS的需求,包括支持数据追踪、质量控制和合规管理。重点讨论选型关键考虑因素,如ISO/IEC 17025兼容性、电子记录防篡改机制、审计追踪功能等。提供实操步骤,从需求分析到实施培训,帮助实验室选择合适软件,确保体系合规并提升运营效率。

实验室负责人资质详解。本文阐述技术负责人和质量负责人的角色、职责及其资质要求,包括教育背景、工作经验、专业技能等方面。基于CNAS-CL01:2018标准和相关管理办法,提供实操指导,帮助实验室满足评审需求,提升管理水平和技术能力。

本文详解CMA资质认定条件,包括法人资格、人员配备、工作场所、设备设施、管理体系运行至少3个月以及法规合规,评审准则涵盖机构主体到管理体系5个方面及远程评审程序,认定手册提供申请书、评审报告、变更表模板及操作指导。基于总局令第47号和2023年第21号公告,帮助实验室高效申请,避免退回风险。
注意:每日仅限20个名额