CMA初次评审、变更评审、复评审、换证评审,一次说明白
CMA初次评审、变更评审、复评审、换证评审详解。本文基于2021管理办法和2024评审准则,一次说明定义、条件、流程和区别,包括初次全面评估、变更针对验证、复评审定期复核和换证到期续期。提供2025年实操建议和问题应对,帮助实验室高效管理资质,确保持续合规运营。

CMA初次评审、变更评审、复评审、换证评审详解。本文基于2021管理办法和2024评审准则,一次说明定义、条件、流程和区别,包括初次全面评估、变更针对验证、复评审定期复核和换证到期续期。提供2025年实操建议和问题应对,帮助实验室高效管理资质,确保持续合规运营。

一份完整的设备校准证书应该包含哪些内容?本文基于CNAS-CL01:2018和ISO/IEC 17025:2017,详解证书12项必备元素,包括机构信息、校准结果、不确定度和溯源声明。提供编制规范、实操步骤和常见问题解决,帮助实验室确保合规,提升评审通过率。

CNAS实验室认可指导详解,包括收费项目(评估体系培训等)、咨询价格(5-20万元)和服务流程(需求评估到获证维护)。基于CNAS-RL01:2025规则,提供选择标准、实操案例和问题解决,帮助实验室高效获证,提升竞争力。

什么是CNAS实验室认可?本文详解CNAS定义、申请条件、流程,以及认可证书的国际互认、法律效力、政府招标加分等用途和价值。基于CNAS-RL01:2025规则,提供2025年实操指导和案例,帮助实验室高效获证,提升竞争力。

什么是合格评定?认证、认可与合格评定的区别详解。本文基于ISO/IEC 17000:2020和CNAS-CL01:2018,解释合格评定作为评估符合性的总过程,认证作为第三方声明,认可作为对评定机构能力的确认。详细对比对象、目的、效力和应用场景,提供实际案例和联系分析,帮助理解这些概念在实验室认证中的作用和意义。

申请CNAS认可对检验检测机构和实验室的六大核心意义(国际互认、法律效力、政府加分等)和八大量化价值(业务增长30-80%、单价提升20-50%等)。2025年最新政策解读+真实案例,帮助机构判断是否申请CNAS以及申请的最佳时机。
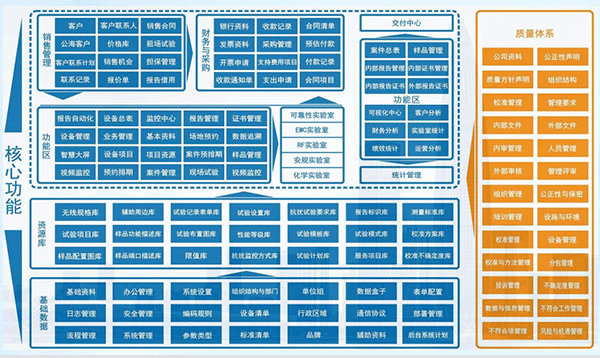
本文详解CNAS实验室LIMS系统选型指南,基于GB/T 27025-2019、ISO/IEC 17025:2017及CNAS-RL01:2025,涵盖ISO兼容、防篡改电子记录、审计追踪、多场所管理等关键功能,及需求评估、调研POC、合同实施等流程,提供避免误区策略,助力实验室缩短3-6个月周期,成功率100%,实现数据追踪效率翻倍,抓住检测市场超5500亿元规模、年增长9%-13%的机遇。

本文提供2026年最新版CNAS实验室申请教程。深度解析ISO/IEC 17025标准下的申请条件(管理体系运行6个月、能力验证要求)、5大详细流程步骤及核心材料清单。结合行业实战经验,提供范围规划、数字化管理(LIMS)及模拟评审等通关策略,助您高效获得国际互认的实验室认可资质。
注意:每日仅限20个名额