实验室资质认定是检测机构获得市场准入资格的关键环节,随着监管要求的不断升级,申请过程中的合规性成为关注焦点。许多实验室在准备阶段对标准理解存在偏差,导致评审周期延长。当前 CMA 认证申请通常遵循严格的流程管理,从提交材料到最终发证,整体周期大约需要 8 至 12 周。若申请材料存在瑕疵,认证部门会在 2 至 3 周内与申请人联系反馈,否则默认材料初审通过。理解这一时间节点有助于实验室合理规划资源,避免因材料反复修改而影响业务开展。
认证周期与材料审核关键点
申请效率很大程度上取决于前期准备工作的充分性。在正式提交申请前,实验室需确保管理体系已运行足够时间,并完成了内部审核与管理评审。材料审核阶段,评审组重点关注文件的完整性与真实性。常见延误原因包括人员资质证明不全、设备校准证书过期或方法验证报告缺失。为避免此类问题,建议建立材料清单核对机制,确保每一份支撑性证据均符合现行准则要求。节假日顺延是周期计算中的常态因素,规划时需预留缓冲时间。
现行标准依据与合规要求
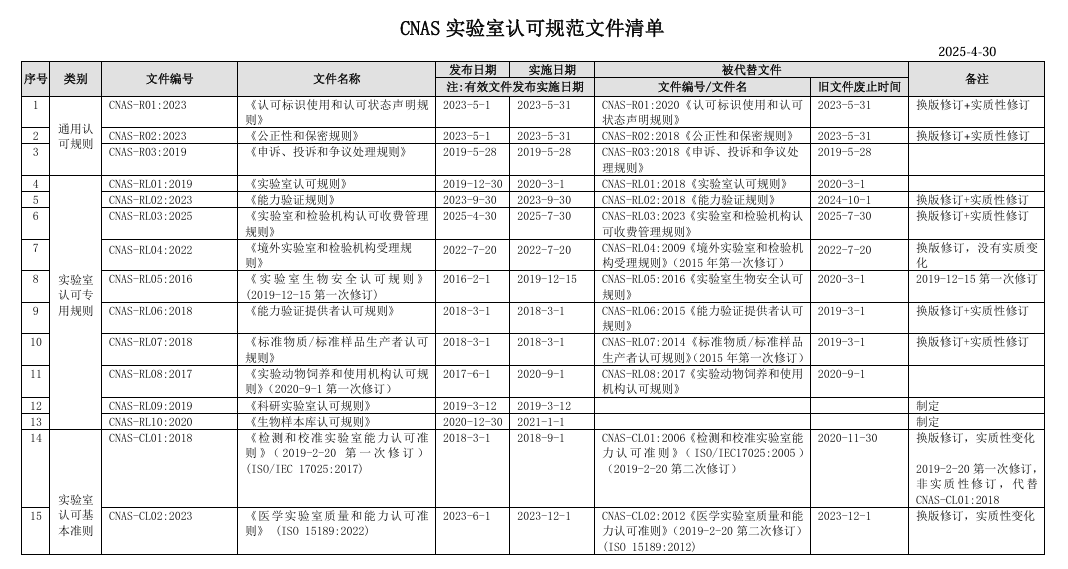
技术能力的评估必须基于有效的标准依据。当前 CMA 评审主要依据 GB/T 27025-2019 及其相关应用说明,该标准等效采用 ISO/IEC 17025:2017,强调了风险管理与公正性要求。实验室需特别注意,旧版评审依据已不再适用,体系文件必须完成换版更新。对于同时申请 CNAS 认可的实验室,还需兼顾 CNAS-CL01:2018 及 CNAS-RL01:2025 的相关规则。双轨运行虽增加工作量,但能显著提升实验室的技术公信力与市场竞争力。
常见不符合项及纠正策略
在正式评审过程中,不符合项的整改是决定能否通过的关键。根据过往案例分析,公正性管理与体系文件执行是高发区域。以下表格汇总了典型问题及应对方向,供实验室自查参考。
| 不符合项类别 | 典型表现 | 纠正措施方向 |
|---|---|---|
| 公正性管理 | 未识别潜在利益冲突 | 完善公正性声明与风险识别记录 |
| 体系文件 | 质量手册与实际操作脱节 | 修订文件并确保全员培训到位 |
| 技术记录 | 原始信息追溯性不足 | 规范记录格式,强化样品流转标识 |
| 设备管理 | 校准周期设置不合理 | 依据使用频率重新评估校准计划 |
申请过程中的疑难解析
针对实验室在准备阶段的高频疑问,以下选取两个典型问题进行解答。这些问题直接关系到申请的成功率,需要管理者高度重视。
问题一:实验室间比对是否必须执行?
虽然标准未强制规定每一次申请都必须提供比对结果,但为了以防万一,建议最好做一下实验室间比对。每个评审组对技术能力的验证方式可能存在差异,具备有效的比对数据能有力证明检测结果的可靠性。特别是在新方法引入或关键设备更换后,比对报告是证明技术能力持续维持的重要证据。
问题二:CNAS 章能否标注非认可项目?
这是一个常见的误区。CNAS 认可标识只能用于认可范围内的项目,严禁超范围使用。在报告编制过程中,必须严格区分认可项目与非认可项目,避免违规标注导致认可资格被暂停或撤销。对于未获认可的项目,可采用其他合规方式说明,但不得使用认可标识。
总结与建议
CMA 认证申请是一项系统性工程,涉及人员、设备、环境及管理多个维度。成功的关键在于对现行标准的准确理解与严格执行。实验室应摒弃侥幸心理,扎实做好体系运行记录,确保所有活动可追溯、可验证。通过提前识别风险点并实施有效纠正,不仅能顺利通过评审,更能借此机会提升内部管理水平,为后续业务发展奠定坚实基础。
德恺咨询专注于实验室技术领域,提供 CNAS 认可与 CMA 认定全流程咨询服务。团队拥有资深评审员背景,熟悉最新评审准则与技术要求,擅长体系文件策划与现场整改指导。我们配备先进模拟评审设备,精准识别潜在风险点,确保客户顺利通过资质认定。欢迎联系专业工程师获取定制化解决方案。